Nuedexta (декстрометорфан хидробромид и хинидин сулфат) е одобрен от канцеларията на Food and Drug Administration (FDA) като първа линия на лечение за неконтролируем смях или плач, медицинско познато като псевдобаларно засягане (PBA), съобщи Avanir Pharmaceuticals Inc. Хората с Pseudobulbar Affect могат да станат твърде емоционални без видима причина; това е неврологично състояние, при което пациентът изпитва неволни, внезапни и чести епизоди на плач или смях. Пациентите с MS (множествена склероза), ALS (амиотрофична латерална склероза), травматични мозъчни увреждания, инсулт, както и някои други неврологични състояния могат да бъдат засегнати с PBA. Епизодите на PBA често се проявяват непропорционално на емоционалното състояние на индивида.
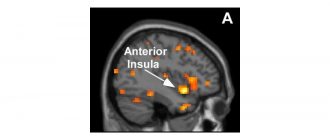
Nuedexta действа върху сигма-1 и NMDA мозъчните рецептори. Точно какви механизми се появяват, за да се намалят епизодите на неконтролирано смях или плач, не са ясни, обясняват експертите. Проведени са клинични изпитвания на участници с MS и ALS. Не е доказана безопасността и ефективността на Nuedexta при пациенти с болест на Алцхаймер и други деменции.
Проучванията показват, че пациентите на Nuedexta са имали значително по-малко епизоди на плач или смях в сравнение с тези на плацебо.
Кийт Каткин, президент и главен изпълнителен директор на Avanir заяви:
Приемането на Nuedexta от FDA отбелязва важен крайъгълен камък за хората, живеещи с PBA, което е недостатъчно признато и изтощаващо неврологично състояние. Одобрението на Nuedexta също така отбелязва прехода на AVANIR към това да стане търговско предприятие, готово да подкрепи успешното стартиране на първото одобрено от FDA лечение за PBA. Очакваме, че Nuedexta ще бъде на разположение по рецепта през първото тримесечие на 2011 година.
Д-р Николай ЛаКрока, Общество-член на МС, заместник-председател на Изпълнителната агенция по здравеопазване и политически изследвания, заяви:
Това одобрение от FDA представлява значителна стъпка напред за хората, които живеят с инвалидизиращите ефекти на PBA. За хората, които изпитват необясними пристъпи на неподходящ смях или плач, тази нова терапия има потенциала да помогне по същество както на тях, така и на техните семейства.
Рандал Кей, д-р, главен медицински директор, Avanir Pharmaceuticals, заяви:
Днешното одобрение на NUEDEXTA е доказателство за убеждението на пациентите и изследователите, участвали в нашите проучвания, и представлява над 10 години научноизследователска и развойна дейност от нашите специалисти. За нас е много удоволствие да доставим първата доказана терапевтична възможност на много пациенти в САЩ, които живеят с PBA. Бих искал да благодаря на FDA за това, че работим в тясно сътрудничество с нас, за да направим NUEDEXTA достъпна.
Д-р Ерик Пиро, Кливланд Клиника, директор на отдела за ALS, също изследовател в клиничните изпитвания Nuedexta, заяви:
ПБА е увреждащо неврологично състояние, често срещано при пациенти с неврологични заболявания или наранявания. Тези пациенти често изпитват неудобство поради непредвидимите си емоционални изблици, което води до нарушаване на междуличностните им връзки и социална изолация. Като лекар, който се грижи за много пациенти с ПББ, се радвам, че сега има безопасна и ефективна възможност за лечение на ПББ, която може да помогне на тези пациенти да възвърнат повече контрол над ежедневния си живот и да живеят с достойнство.
Пациентите с ПБА често са неправилно диагностицирани с депресия. Пациентите с ПБА с непредсказуеми и неволни изяви на емоции може да станат тревожни и изключително неудобно, особено когато има много хора наоколо. В някои случаи индивидът може да избегне социални ситуации. Този умишлен ход към изолация може да изглежда като признак на депресия. Въпреки това, някои пациенти имат както PBA, така и депресия.
Според Avenir, над 1 милион американци са умерено или силно засегнати от PBA.
Avenir, в своя уеб сайт PBA пише:
Въпреки че ПБА е вторична за неврологичните заболявания и мозъчните увреждания, това е отделно неврологично разстройство, което може да бъде диагностицирано и лекувано отделно от основното неврологично заболяване или увреждане.
Източник: Avenir Pharmaceuticals Inc.
Написано от Christian Nordqvist