Изследователите разработват нов метод за по-ефективно унищожаване на рака. Тяхната стратегия "гладува" тумори, лишава ги от основното хранително вещество, което те изискват да растат и да се разпространят.

Глутаминът е аминокиселина, която се намира изобилно в нашите тела, особено в кръвта и костната тъкан. Основната му роля е да поддържа синтезата на протеините в клетките.
За съжаление, обаче, глутаминът също е ключово хранително вещество за много видове ракови тумори, които са склонни да "консумират" повече от тази аминокиселина, защото клетките им се делят по-бързо.
Ето защо изследванията разследват възможността за блокиране на достъпа на раковите клетки до глутамин като нов терапевтичен подход при лечение на рак.
Чарлз Манинг и няколко други изследователи от Центъра за молекулярни проби на "Вандербилт" в университета "Вандербилт" в Нешвил, Тенеси, сега успяха да се справят с пробив в растежа на туморния тумор.
За целта те използват експериментално съединение, наречено V-9302, за да блокират усвояването или абсорбцията на глутамин от ракови клетки. Констатациите на изследователите бяха публикувани тази седмица в списанието
"Раковите клетки проявяват уникални метаболитни изисквания, които ги разграничават биологично от здрави клетки. Метаболитната специфичност на раковите клетки ни дава богати възможности да разделим химия, радиохимия и молекулярно изображение, за да открием нова ракова диагностика, както и потенциални терапии".
Чарлс Манинг
Новото съединение инхибира глутаминния носител
Изследователите обясняват, че глутаминът се пренася през тялото и се "храни" с ракови клетки чрез аминокиселинния транспортер ASCT2 – вид протеин.
"Повишените нива на ASCT2 са свързани с лошата преживяемост при много човешки ракови заболявания, включително белодробни, гръдни и дебело черво", отбелязват учените в въведението си.
Въпреки това проучвания, които са успели да заглушат гена, който кодира ASCT2 – ген SLC1A5 – са успели да намалят растежа на туморите на рака.
Подтикнати от това познание, Манинг и колегите си тръгват да проектират особено силен инхибитор на ASCT2, съединението V-9302. Изследователите изследват съединението върху раковите клетки, култивирани в мишки, както и използването на ракови клетъчни линии, разработени в лабораторията, in vitro.
Аминокиселинният транспортен инхибитор успя да намали растежа на раковите клетки и да намали способността им да се разпространява чрез "повишаване" на оксидативния стрес на раковите клетки, което води до тяхната евентуална смърт.
"Тези резултати не само олицетворяват обещаващия характер на водещото съединение V-9302, но и подкрепят концепцията, че антагонизирането на [разрушаването] на метаболизма на глутамин на ниво транспортер представлява потенциален жизнеспособен подход в прецизната ракова медицина", заключават изследователите в своята статия.
Иновации в изображенията с ПЕТ на хоризонта
В същото време авторите отбелязват, че за да се лекуват пациенти с тумори, които разчитат на глутамин да расте и да се разпространява в бъдеще, "този нов клас инхибитори ще изисква валидирани биомаркери".
Това означава, че изследователите ще трябва да развият начин, по който те ще могат да разберат колко ефективно инхибиторът действа върху протеина или колко малко от глутамина достига раковите клетки накрая. Това е така, защото производството на ACST2 и нейната активност вероятно ще са различни за всеки индивид.
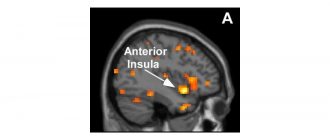
За да се справим с този проблем, Манинг и екипът препоръчват да се използват маркери за позитронна емисионна томография (PET), които ще открият туморни тумори, като открият каквото и да е увеличение на скоростта на метаболизма на глутамина, което ще бъде по-високо в сравнение с нормалните здрави клетки в организма.
В центъра "Вандербилт" за молекулярни проби сега се провеждат пет клинични изпитвания, предназначени да тестват ефективността на 18F-FSPG – нов радиофармацевтик – т.е. радиоактивен медикамент, използван при PET изследвания – за проследяване на различни видове ракови тумори, включително белодробни, яйчниците и рак на дебелото черво.
Екипажът и екипът провеждат и тестове на 11С-глутамин – метаболитен тракозер за глутамин. Освен това изследователите могат да използват молекулярен проследяващ агент, за да потвърдят дали протеин инхибиторът действително достига целта си.
– Не би ли било провокативно – отправя се Манинг, – ако можехме да направим следене на PET на базата на определен наркотик, който да ни помогне да предвидим кои тумори ще натрупат наркотика и следователно да бъдем клинично уязвими към нея?
"Това е самата същност на" визуализираната "прецизна ракова медицина – той ентусиазира.