Бактерията, която е основната причина за некротизиращ фасциит или заболяване, причиняващо плът, причинява широко разпространена смъртоносна инфекция, като накара нервната система да спре имунната система да я атакува.
Екип, ръководен от учени от Харвардското медицинско училище в Бостън, Масачузетс, направи изненадващо откритие, докато изучава тактиките за стимулиране на заболяването при мишки с некротизиращ фасциит.
Можете да прочетете за изследването в документ, който скоро ще бъде публикуван в списанието, където изследователите предлагат и две потенциални лечения.
Ако успеят в опити с животни и хора, леченията могат да имат огромна стойност при "високо инвазивните бактериални инфекции".
"Некротизиращ фасциит", обяснява старшият изследовател Исак М. Чиу, който е асистент по микробиология и имунология в Харвардското медицинско училище, "е опустошително състояние, което остава изключително предизвикателно за лечение и има неприемливо висок процент смъртност."
Болестно хранене
Болестта, която яде месо, е причинена от сериозна бактериална инфекция на подкожната тъкан, тъканта, която лежи точно под кожата, и фасцията, тъканта, която покрива органите, които лежат в тялото.
Болестта е много рядка; всяка година засяга приблизително 200 000 души по света, което включва около 1 200 души в Съединените щати.
Инфекцията, която може да бъде причинена от няколко вида бактерии, не е лесна за диагностика и може да се развие внезапно и да се разпространи бързо. Ако не бъде лекувано незабавно, това може да доведе до "многоклетъчен отказ и смърт", което се случва в около 30% от случаите.
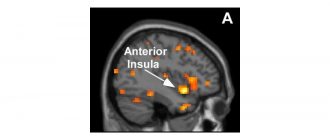
След нараняване, нервната система изпраща един сигнал към мозъка и друг към имунната система. Първият сигнал предизвиква усещане за болка, а вторият указва на имунната система да се задържи.
Учените предполагат, че невроните или нервните клетки имат тази способност да инструктират имунната система да се задържи, за да се предотврати "прекомерното разгръщане" на имунните клетки, което може да причини "обезпечение" на здрави тъкани.
Проф. Чиу става заинтересован от това как това взаимодействие на нервната система и имунната система може да работи при заболяване на плътта, когато открива, че засегнатите пациенти често изпитват прекомерно ниво на болка, настъпващо преди появата на симптомите.
Може би бактерията по някакъв начин е използвала тази естествена двойна реакция на нараняване, за да потисне имунната система за своя собствена полза?
Бактериалният токсин задейства имунното заглушаване
За да проучи по-нататък, той и колегите му разработиха миши модел на болестта, която яде месо, чрез инжектиране на животните с бактериите, взети от инфектирани човешки пациенти.
Използвайки модела на мишката, те откриват, че токсинът, произвеждан от бактерията – известен като стрептолизин S – е бил причина за болка и последващо заглушаване на имунната система.
При по-нататъшни тестове те инжектират мишки с бактерии, които са били генетично конструирани така, че да не могат да произвеждат токсина. Въпреки, че са заразени, мишките не показват обичайната болка и нито инфекцията стана инвазивна.
Изследователите потвърждават ролята на стрептолизин S чрез "преработване" на способността за продуциране на токсини обратно в модифицираните бактерии и след това им се въвеждат в една и съща мишка. Инфекцията се развива в "пълноценно" заболяване, което яде месо.
След това екипът даде на мишките антитяло, което блокира токсина. Симптомите на болката при мишките са много понижени, което потвърждава, че бактериалният стрептолизин S е спусъка.
Основни молекулярни механизми
Изследователите извършиха допълнителни експерименти, в които изследваха основните молекулярни механизми на взаимодействието между нервната система и имунната система.
В тези те открили, че стрептолизин С задейства неврони, за да изпрати болезнен сигнал към мозъка. Това също така задейства друг сигнал към имунната система, който я кара да секретира невротрансмитер или химически посланик, наречен пептид, свързан с ген на калцитонин (CGRP), който след това задържа имунния отговор.
Те също установиха, че CGRP прави това чрез спиране на изпращането на неутрофили и чрез блокиране на способността им да убиват бактериите на мястото на раната.
"Ефективно", отбелязва професор Чиу, "този невронен сигнал заглушава алармената система, която обикновено привлича болните от инфекции на организма, за да ограничат инфекцията".
Той продължава да обяснява, че такъв отговор е подходящ, когато раната е чиста и не е заразена – не искате имунната система да идва и да възпалява здравата тъкан в опит да се справи с инфекция, която не съществува там.
Но бактерията стрептокок се възползва от това и се позовава на същата стратегия, когато раната е заразена, което позволява на болестта да се развива безпрепятствено.
Пациентите в ранен стадий на некротизиращ фасциит често усещат огромно количество болка, но не показват симптомите, които може да се очаква да го придружат – като зачервяване, подуване и възпаление.
Професор Чиу и колегите обаче предполагат, че това бихте очаквали, ако по някаква причина не са призовани неутрофилите, които предизвикват възпалението и се отърват от бактериите.
Два възможни начина за спиране на болестта
След това учените извървяха още един набор от експерименти, в които въведоха бактериите в две групи мишки: една, в която те спряха способността на нервните влакна да носят болезнени сигнали и друг, в който не бяха.
Те показаха, че блокирането на болките в нервите подобрява контрола на организма върху инфекцията.
Различни експерименти, при които мишките са инжектирани с ботулинов невротоксин А – нервен блокер, който се намира в козметичните терапии за лице против бръчки – показаха, че такъв подход може да работи като лечение на заболяване, което яде месо.
Инжекциите на нервния блокер дори 2 дни след като мишките са били заразени за първи път и вече са имали рани, спирали заболяването, причинявайки по-голяма тъканна повреда.
Изследователите също изпробваха друг възможен начин за борба с болестта. Те показаха, че CGRP-блокерите премахват спирачките на имунната система, като спират нервните клетки да изпращат сигнали за спиране. Те също така прекратяват некротизиращия фассит от разпространение при мишки.
"Нашите открития разкриват изненадващата нова роля на невроните в развитието на тази болест и сочат обещаващи контрамерки, които изискват по-нататъшно проучване".
Проф. Исак М. Чиу